Prof. Dr. Mustafa Arda
Ankara Üniversitesi Veteriner Fakültesi
Temel Mikrobiyoloji 1
01.Genel Bilgiler
02. Virusun %50 İnfektif ve Letal Titrelerinin Belirlenmesi
03. Serum Nötralizasyon Titresinin Tayini (%50 Nötralizan Titre)
01.Genel Bilgiler
İzole edilen virusların karakterize veya identifiye edilebilmesi ve üzerinde güvenli çalışmaların yapılabilmesi için, izolatların çeşitli yönleri ile çok iyi bilinmesine ve bütün parametrelerinin saptanmasına gerek vardır. Bunlar belirlendikten sonra, ancak, o virus çeşitli testlerde ve araştırmalarda (bağışıklık testlerinde, aşıların kontrollerinde, hazırlanmalarında, hastalıkların teşhisi için antikor taramalarında ve diğer testlerde) kullanılabilir ve alınan sonuçlara güvenilebilir. Bugün, bu amaca yönelik çeşitli ülkelerde referans laboratuvarlarları bulunmakta ve bunların yardımı ile virusların identifikasyonları yapılmaktadır. Ancak, bu laboratuvarın da, kendisine gönderilen izolatları karakterize ederken infektif titrelerini ve diğer parametrelerini saptaması gereklidir.
Bu amaçla, yapılması ön planda bulunan çalışma, virusun titresinin saptanması ile virus suspansiyonunda ne miktarda, infektif veya letal dozun ve gerekirse plak forming ünitenin (pfu) bulunduğunun kesinlikle belirlenmesidir. Doğaldır ki, bu işlemlerin yapılması oldukça zaman alıcı, titizlik ve beceri isteyen bir konudur.
İlk önce, virusları üretebilmek için gerekli olan canlı sistemlerin belirlenmesi ve bunların izolatın karakterine göre saptanmasıdır. Bu amaçla, embriyolu yumurtalar, hücre kültürleri ve deneme hayvanları kullanılır. Deneme hayvanlarının SPF (specific pathogen free (belli hastalık ajanlarını vücutlarında taşımayan ve kanlarında da spesifik antikor bulunmayan sertifikalı ve özel koşullarda yetiştirilen laboratuvar hayvanları) karakterinde olmaları, hayvanların yaşı, cinsi ve cinsiyetinin ve inokulasyon yollarının iyi ayarlanması gereklidir. Aynı koşullar, embriyolu yumurtalar için de geçerlidir. Şöyle ki, SPF özelliği taşıyan yumurta embriyolarının olması, beyaz kabuklu yumurtalar, embriyoların yaşı, inokulasyon yolu, inokulum miktarları titizlikle seçilmelidir. Hücre kültürlerinin de, türü (epitel, fibroblastik, vs), hayvan orijini (fare, kobay, tavşan, vs) ayrıca, devamlı ve cell-line durumları, üretme besi yerleri ve diğer koşulları oldukça önemlidir. Çok masraflı, yorucu ve özel uzmanlık isteyen böyle konularda özel ve güvenilir organizasyonlardan (hücre bankaları, SPF yumurta ve deneme hayvanları yetiştiren işletmeler) yararlanmak gereklidir. Belirtilen koşulları taşımayan canlı sistemlerin kullanılması, çalışmalara olumsuz yönde etkiler ve denemeleri yanlış sonuçlara götürür.
Yukarıda bahsedilen hususların yanı sıra, izolatların kontamine olmamaları (bakteri, mantar, virus'la), laboratuvarların yeterli, deneyimli personele ve malzemeye ve ayrıca, canlı sistemleri sağlayabilecek ve idame edebilecek parasal desteğe ve ünitelere sahip olması sayılabilir.
02. Virusun %50 İnfektif ve Letal Titrelerinin Belirlenmesi
Virusların infektif veya letal titrelerin belirlenmesi, kullanılan canlı sistemlerde oluşturdukları infeksiyon hastalık veya ölümlere göre hesaplanır. Ancak, hücre kültürlerinde, genellikle, infektif titre belirlenir ve in vitro test olarak kabul edilir. Laboratuvar hayvanlarında yapılan testler in vivo ve embriyolardakiler ise in ovo olarak değerlendirilir. Ancak, in vivo çalışmaların dışındakiler genel olarak eks vivo olarak ta tanımlanmaktadır.
Virusların canlı sistemlerdeki %50 infektif titre (İT50) ve %50 letal titre (LT50) leri belirlendikten sonra, %50 infektif doz (İD50) ve %50 letal doz (LD50) ları da saptanır. İnfektif titre veya letal titre, virusun canlı sistemlerde oluşturduğu %50 pozitif reaksiyonların (infeksiyon, ölüm, CPE, vs) görüldüğü son dilusyonudur (son noktadır). İnfektif veya letal dozlar ise virus suspansiyonu içinde bir inokulum miktarında bulunan virus ünitesini ifade eder ki bu da, infektif veya letal titrelerin pozitif logaritmasıdır. Ancak, bu değerlerin daha belirgin daha yararlı olabilmesi için, kullanılan inokulumun ve canlı sistemlerin de birlikte yazılması gereklidir. Örn, fareler için FİT50 / 0.1 ml veya FLD50 / 0,05 ml, embriyolar için FLD50 / 0.1 ml., doku kültürleri için de DKİD50 / 01ml ve ayrıca plak forming üniteler için de pfu/0.1 ml gibi.
Laboratuvarlarda titrelerin veya diğer parametrelerin tayininde genellikle, temin ve bakımının kolay olması, fiyatının ucuz ve fazla yer işgal etmemesi vs gibi nedenlerle hücre kültürleri fazla kullanılır ve bunlarda oluşan morfolojik değişiklikler ve dejenerasyonlara (sitopatik efektler, CPE) ve bazen de, plaklara göre değerlendirmeler yapılır. Diğer canlı sistemler de gerektiğinde kullanılabilir.
Titre tayininde viruslar, genellikle, uygun bir diluent (FTS, buffer vs.) içinde 2-5 veya 10 katlı olarak sulandırılır. Bir örnekle infektivitenin tayininin yapılması aşağıda açıklanmaktadır:
Örnek-1: Virusun (Newcastle, Influenza, vs) uygun diluent içinde 10 kıtlı sulandırmaları yapıldıktan sonra, kritik dilusyonlardan (10-8, 10-7, 10-6, 10-5), her birinde iyi üremiş monolayer duyarlı hücre bulunan tüplere (her dilusyondan 6'şar tüpe) 0.1 ml. miktarlarında ekim yapılarak, uygun ısı ve sürede inkubasyonda tutulurlar. Tüpler, mikroskop altında kontrol edilerek oluşan CPE'ler (pozitif reaksiyonlar) saptanır. Alınan sonuçlar aşağıda gösterilen tablodaki gibi belirlensin:
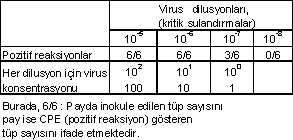
Yukarıdaki tabloya göre virus, 10-5 ve 10-6 dilusyonlarında, ekilen 6 hücre tüpünün hepsinde (6/6) CPE oluşturmuş (poz.reak,) buna karşın 10-7 de, ekilen 6 tüpün 3 tanesinde 3/6) ve 10-8 de hiçbir tüpte CPE gözlenememiştir (0/6).
Çizelgeye göre, virusun %50 infektif titresi, tüplerin %50'sinde CPE (pozitif reaksiyon) görüldüğü dilusyondur (10-7). Virus bu dilusyonda bir inokulum miktarında (0.1 ml.), sadece bir tane %50 infektif doza (1 DKİD50/0.1 ml) sahiptir ve bu sulandırma da aynı zamanda virusun hücre kültürlerindeki infektif titresini oluşturur (10-7DKİT50). Bu dilusyonda virus, ekilen 6 tüpün 3'ünde, yani %50'sinde CPE meydana getirmiştir.
Bu noktadan başlayarak yoğun sulandırmalara yani sola doğru gidildiğinde, 10-7'den 10 defa daha yoğun virus bulunan 10-6 da 10 (101) ve 100 defa daha yoğun olan 10-5 de de 100 (102) ve hiç sulandırılmamış olan virus suspansiyonunda da 107 (10 000 000) DKİD50/0.1 ml bulunacak demektir. Diğer bir ifade ile, infektif titrenin (10-7), pozitif logaritması (107)dır. Bu duruma göre virusun hiç sulandırılmamış suspansiyonda, 0.1 ml. inokulum miktarında 107 (10 milyon) DKİD50 bulunmaktadır. Bu hesaplama tarzı aynen, embriyolu yumurtalar ve deneme hayvanları için de geçerlidir.
Ancak, pratikte 6 hücre tüpü (yumurta veya deneme hayvanı) yerine genellikle 5 tane tüp kullanıldığı gibi, %50 titre de her zaman 3/6 ya rastlamaz ve 2/6 veya 4/6 da olabilir. Böyle durumlarda bazı formüllerden yararlanarak %50 titre hesaplanır. Bu formüller arasında en fazla kullanılan Reed ve Muench ile Kaerber yöntemleri bulunmaktadır.
| Örnek-2: Virus (Newcastle, Influenza, vs) bir diluent içinde 10 katlı sulandırılarak, kritik son 5 dilusyonunun her birinden ayrı ayrı 5'er hücre tüplerine ekilmiş, uygun bir ısı ve inkubasyon süresinde gözlenen CPE (poz.reak.) aşağıdaki tabloda gösterilmiştir. Buna göre %50 infektif titrenin ve infektif dozun hesaplanması kısaca şöyledir. |
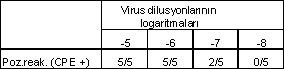 |
Yukarıdaki çizelgeye göre virusun %50 infektif titresi, 10-6 ili 10-7 sulandırılmaları arasına isabet etmekte ve bu nokta 10-7 ye daha yakın bulunmaktadır. Bu %50 noktanın hesaplanmasında her iki yöntem de kullanılarak değerlendirme yapılacaktır. Ancak, hesaplamaya başlamadan önce, yukarıdaki çizelgeden yararlanarak, aşağıda gösterildiği gibi ikinci bir tablo hazırlanarak kümülatif değerler de belirtilecektir. |
 |
I) Reed ve Muench Metoduna Göre %50 son Noktanın Hesaplanması
Bu yöntemde, aşağıdaki belirtilen formülden yararlanılır.
Yapılacak işlemler sıra ile:
1) Orantısal uzaklık hesaplanır (OU)
%50'nin üstündeki poz.reaklar -%50
OU= ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾
%50'nin üstündeki poz.reaklar - %50'nin altındaki poz.reakl.
Çizelgede belirtilen değerler formülde yerine konulur (son kolon)
100-50 50
OU = ¾¾¾¾¾ = ¾¾¾¾ = 0.833
100-40 60
2) Bulunan orantısal uzaklık değeri (0.833), dilusyonlar arası katsayının logaritması (10 katlı sulandırma yapıldığı için, 10'un log., 1'dir) olan 1'le çarpılır.
0.833 x log1010 = 0.833 x 1 = 0.833
3) Bulunan değer (0.833), %50 noktasının üstündeki ilk dilusyonun logaritmasına ilave edilir.
-6.000
0.833
¾¾¾¾
-6.833
Bu denemeye göre virusun doku kültürlerindeki titresi (%50)r 107 DKIT50 / 0.1 ml'dir.
Bu bulguya göre, virusun hiç sulandırılmamış suspansiyonunda 106.833 DKİD50 / 0.1 ml. infektif doz bulunmaktadır. Bu logaritmik sayının aritmetik değerini bulmak için, bunun anti logaritmasını almak gerekir. Bu da ya hesap makineleri yardımı ile veya logaritma cetvelinden bulunur. Bu sayı da 7 rakamlı olacağından, 1/6880000 dir. Buna göre de virusun hiç sulandırılmamış suspansiyonundaki infektif dozu, 0.1 ml'de, 6880000 DKİD50 (688 x 104 DKİD50 / 0.1 ml)dir.
II) Kaerber metoduna göre hesaplama
Bir önceki çizelgeden yararlanarak, elde edilen bulguları bu yöntemde de kullanmak mümkündür. Hesaplamada kullanılacak formül şöyledir.
%50 infektif doz (İD50) = m-d (S-0.5)
Bu formüldeki semboller:
m= %100 poz.reak. görülen dilusyonun negatif logaritması (-6)
d= İki dilusyon arası katsayının logaritması (log1010=1)
S= Her dilusyona ait pozitif reaksiyonların toplamı /100
0.5 = Sabit değer
Çizelgede, son sütundaki değerler, formülde yerine konursa,
100 + 40 + 0
İD50 = (-6) - (1) (¾¾¾¾¾¾ - 0.5 ) = -6-1 (0.9)
100
İD50 = -6.9
Görüldüğü üzere, Kaerber metoduna göre de virusun %50 infektif titresi 10-6.9 dur. Her iki yöntem arasında önemli bir fark bulunmamaktadır. Diğer işlemler aynen Reed ve Muench metodunda olduğu gibidir.
Her iki yöntemle saptanan titre veya dozların, %95 güvenle, minimal ve maksimal sınırlarının belirlenmesinde, Standard hatanın (Sh) saptanması gerecektir. Bu amaçla da aşağıdaki formülden yararlanılır,
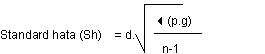
Bu formüldeki semboller:
d = Dilusyonlar arası katsayının logaritması (log1010 = 1)
p = Pozitif reaksiyonların yüzde (%) oranı
q = 1-p
n = Denemede kullanılan hücre kültür tüp sayısı (her dilusyon için)
å = Toplama işareti
| Bu sembollerin değerlerini belirleyebilmek için, aşağıdaki tarzda yeni bir çizelge yapmak gerekecektir. | 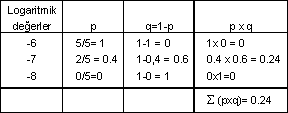 |
Saptanan değerler formülde yerine konur,
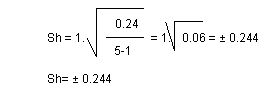
Bu bulgulara göre infektif titre 10-6.833 ± 0.244 olarak belirlenmiştir. Virus titresinin (%95 güvenle serbestlik derecesi, SD = 5-1 = 4 ve t-tablosunda değeri 2.57'dir) alt ve üst sınırları,
Üst limit = -6.833 ± (2.57 x 0.244) = -7.460
Alt limit = -6.833 - (2.57 x 0.244) = -6.206
olacaktır. Bunun anlamı, deneme bir çok kez yapılsa, %95 güvenle, titre, -6.206 ile -7.460 arasında değişecektir. Bu sınırların dışında olma olasılığı %5'dir.
Virusun iki katlı sulandırıldığı durumlarda yapılacak işlemler
| Örnek 3: Virus, iki katlı (1/10,1/20, 1/40,1/80,.....1/320) sulandırıldıktan sonra her bir dilusyondan 5'er tane doku kültürü tüpüne (veya embriyolu yumurtalara) 0.1 ml miktarında ekilir. Uygun bir süre ve ısıda inkubasyondan sonra hücrelerdeki CPE'ler gözlenir ve bunlara dayanarak aşağıdaki kümülatif değerleri belirten çizelge hazırlanır. |
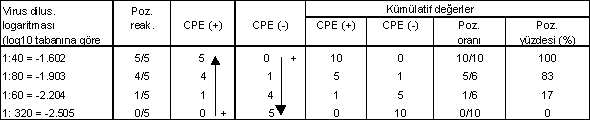 |
Reed ve Muench metoduna göre alınan sonuçların değerlendirilmesi:
83-50 33
1) Orantısal uzaklık (OU) = ¾¾¾¾ = ¾¾ = 0.50
83-17 66
2) Bu örnekte, virus iki katlı sulandırıldığı için, katsayı 2'dir ve bunun logaritması da 0.301'dir. Buna göre,
0.50 x 0.301 = 0.150
3) Bu son değer, %50'nin üstündeki ilk dilusyonun logaritmasına eklenir.
1/80'nin Log10'a göre değeri -1.903'dür.
-1.903
0.150
¾¾¾¾
-2.053
Buna göre, virusun %50 infektif titresi 10-2.053'dir. Bunun sayısal ortak değeri 1/113'dür. Virus bu dilusyonda, 0.1 ml. inokulum miktarında bir tane %50 infektif doza sahiptir. Hiç sulandırılmamış virus suspansiyonunda ise, 0.1 ml'de 113 DKİD50 (113 DKİD50/0.1 ml) bulunacaktır.
Eğer bulgular, Kaerber yöntemine göre hesaplanırsa aynı sonuç bulunacaktır.
Eğer, virus sulandırılmaları, 5 katlı olarak (1/5,1/25,1/125,......) yapılırsa, burada da orantısal uzaklık sonucu, sulandırma katsayısı olan 5'in logaritması, 0.698'le çarpılması gerekir.
03. Serum Nötralizasyon Titresinin Tayini (%50 Nötralizan Titre)
Bireylerin kanlarında, aktif ve/veya pasif bağışıklık sonucunda oluşan veya bulunan spesifik antikorların (genellikle, İgG, İgM, İgE) ortaya konularak, bunların yeterli düzeyde olup-olmadıklarının belirlenmesi insan ve veteriner hekimlikte çok önemli yeri vardır. Günümüzde geliştirilen yeni aletler ve yöntemler yardımı ile özgül antikorları ortaya koymak ve kısa bir zaman süreci içinde çok sayıda şüpheli serumu değerlendirmek mümkün olabilmektedir. ELISA (makro ve mikro teknikler), bu amaç için rutinde kullanılan en duyarlı, güvenilir ve hızlı metotların arasında yer almaktadır.
Aynı amaç için eskiden kullanılan in vivo (laboratuvar hayvanları), in ovo (embriyolu yumurtalar) ve in vitro (hücre kültürleri) gibi canlı sistemler yardımı ile serumların %50 nötralizan titrelerinin belirlenmesi teknikleri, zaman alıcı, yorucu, masraflı, deneyimli personele gereksimi olması gibi nedenlerle, bugün artık rutin çalışmalarda yer almamakta ancak özel amaçlar için araştırıcılar tarafından, çok az da olsa kullanılmakta ve daha ziyade hücre kültürleri ve çok az olarak ta deneme hayvanları uygun görülmektedir.
Nötralizasyon testlerinde de sonuçlar pozitif reaksiyonlara göre (ölen, infeksiyon, CPE+) değerlendirilmektedir. %50 nötralizan titrenin belirlenmesinde de, yine, Reed ve Muench ile Kaerber'in, ancak, daha değişik formüllerinden yararlanılmaktadır.
Nötralizasyon testlerinde, serumların içindeki antikor tipleri belirlenmez, buna karşın, serumun, belli virus konsantrasyonuna karşı, canlı sistemlerdeki koruyucu %50 nötralizan titreleri saptanır ve buna göre serumların etkinlikleri değerlendirilir.
Nötralizasyon testlerinde, her ne kadar araştırıcılara göre değişirse de, genellikle, virus belli dozda (100-250 veya 500 DKİD50/0.1 ml de veya ELD de) sabit tutularak, şüpheli serumların iki katlı (1:2, 1:4, 1:8,..................1:512 veya 1:5, 1:10, 1:20,......1280) sulandırmaları yapılır ve bunların 0.1 ml miktarları steril tüpler içinde belli ısı ve sürede karıştırılarak tutulur ve sonra canlı sistemlere ekilerek, CPE'ler veya infeksiyon-ölümler (pozitif reaksiyonlar) yönünden değerlendirilirler. Serum sulandırmaları iki katlı yapılabileceği gibi, hastalığın özelliğine göre, 5 veya 10 katlı olarak ta dilue edilebilirler.
Nötralizasyon testlerinde canlı sistemlerdeki pozitif reaksiyonların görülüş sırası, virusun infektif veya letal titrelerinin tayininde ortaya çıkanların (pozitif reaksiyonların) tersi yönündedir. Çünkü, serumun yoğun dilusyonlarında antikor miktarının fazla olması (eğer pozitif serumlar ise), virusun sabit tutulan dozunu her zaman nötralize eder ve canlı sistemlerde de pozitif reaksiyonlar gözlenemez. Ancak, serumun ileri sulandırmalarında, içinde antikor azalacağından, virus tam olarak nötralize edilemez ve ortamda kalan aktif virusun varlığı nedeniyle pozitif reaksiyonlar görülmeye başlar: Örn, virus titrasyonlarında virusun ilk (yoğun) dilusyonlarında, poz. reak. oranı, 5/5 iken, nötralizasyon testlerinde ise pozitif serumun ilk (yoğun) sulandırmalarında, 0/5'dir.
Klasik nötralizasyon testleri laboratuvarlarda başlıca iki metottan birisi ile yapılmaktadır.
1) Virus sabit tutulur (belli infektif veya letal dozda), test edilecek şüpheli serumlar sulandırılır (2-5 veya 10 katlı).
2) Virus sulandırılır (2-5 veya 10 katlı), serum sabit tutulur (1:5 veya 1:10 yoğunluğunda)
Genellikle birinci yöntem daha fazla tercih edildiğinden, burada da bu metot daha ayrıntılı ve örneklerle anlatılacaktır.
Serumların %50 nötralizan titreleri, sabit virusun infektif veya letal etkisini %50 önlediği, son dilusyonlarıdır. Testin bir örnekle açıklanması ve sonuçların değerlendirilmesi:
Örnek 3: Virus (Newcastle, Influenza, vs), 250 DKİD50/0.1 ml'de sabit tutulur (virusun 0.1 ml'inde 250 DKİD50 olacak tarzda sulandırması yapılır) ve test edilecek steril şüpheli serumlar (pozitif ve negatif kontrol serumlar da dahil) iki katlı (1:2, 1:4, 1:8,......1:512) ayrı ayrı sulandırılır. Her serum dilusyonundan 0.5 ml alınarak ayrı tüplere konulur ve üzerlerine de sabit virustan 0.5 ml ilave edilerek iyice karıştırılır ve oda ısısında (veya inkubatörde veya değişik derecelerde) 45 dakika bekletilir. Bu sürenin sonunda, her bir karışımdan (virus + serum) 1 ml. alınarak, 5 doku kültürü tüpünün her birine 0.2 ml. inokule edilir ve hücreler üzerine iyice temas etmesi sağlanır. Tüpler inkubatöre yerleştirilir. Burada, uygun ısı ve süre kaldıktan ve her gün mikroskop altında hücrelerdeki CPE'ler yönünden kontrol edildikten sonra, sonuçlar, aşağıdaki tarzda bir çizelge halinde düzenlenmiştir.
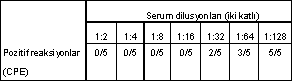
| Çizelgede görüldüğü üzere, serumun yoğun sulandırmalarında (1:2'den 1:16'ya kadar) içinde antikor miktarı fazla olduğundan sabit virusu nötralize etmiş ve hiç bir CPE gözlenememiştir. Diğer bir ifade ile, bu dilusyonlarda hücrelerde hiç bir CPE bulunmamakta ve hücreler normal görünümlenir. Pozitif reaksiyon oranı 0/5'dir. Buna karşın, 1:32 serum dilusyonunda 2 tüpte CPE + (2/5). 1:64 dilusyonda 3/5 ve 1:128'de de 5 tüpte CPE gözlenmiştir (5/5). Bu durum kümülatif değerleri ile birlikte, aşağıda, ikinci bir tabloda belirtilmiştir. |
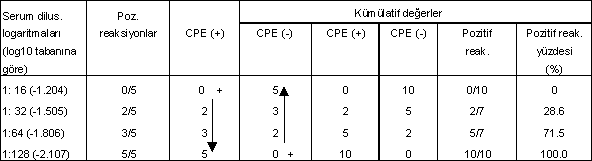 |
Bu çizelgeye göre bir serumun %50 nötralizan titresi, 1:32 ile 1:64 dilusyonları arasında bulunmaktadır. Bu son noktanın belirlenmesinde yararlanılacak formüller ve hesaplama tarzı kısaca şöyledir.
1) Reed ve Muench Metodu
%50 - %50'nin altındaki poz.reak.
%50 nötralizan titre (NT50) = ¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾¾
%50'nin üst.poz.reak.- %50'nin altındaki poz.reak.
Tabloda belirtilen değerler formülde yerine konur
50-28.6 21.4
1) OU = ¾¾¾¾¾ = ¾¾¾¾ = 0.498
71.5-28.6 42.9
2) 0.498 x 0.301 = 0.149
3) 1/32'nin logaritması - 1.505
-1.505
0.149
¾¾¾¾
-1.654
Buna göre serumun %50 nötralizan titresi 10-1.654 dür. Bu değerin anti logaritması. 1/45 dir. Test serumu, 1/45 dilusyonunda, bir inokulum miktarında (0.1 ml.de), virusun sadece bir tane 250 DKİD50 sini nötralize edebilecek antikora sahiptir. Buna karşın hiç dilue edilmemiş serumda, 0.1 ml.de, 101.654 veya 45 tane 250 DKİD50 virusu nötralize edecek antikor bulunur.
Ancak, bulunan bu değerin, serumun pozitif veya negatif olup olmadığını ortaya koyabilmesi için, önceden, aranan infeksiyon için, negatif serumlara göre belirlenen bir negatiflik kriterinin saptanması şarttır. Ayrıca, bilinen pozitif ve negatif serumların da teste dahil edilmesi ve bunların da normal çalışması gereklidir.
II) Kaerber Metodu
Tablodaki aynı sonuçlardan yararlanılarak aşağıdaki formül kullanılır.
h (å p + n/2)
NT50 = do - ¾¾¾¾¾¾¾¾
n
Bu formüldeki semboller:
do = Sıfır pozitif reak.gösteren serum dilusyonlarının logarit. (1:16 = 10-1.204)
h= Dilusyonlar arası katsayının logaritması (log10 2 = 0.301)
n= Her dilusyon için kullanılan tüp sayısı (n = 5)
å p= Poz.reak.ların toplamı (%100 poz. ve %100 neg. olanlar hariç)
1:32 de 2 tüp ve 1:64 de 3 tüp de CPE + olgu görülmüş olup toplam 5 tüp (åp= 5).
Bulunan bu değerler formülde yerine konulur.
0.301 (5 + 5/2)
NT50 = -1.204 - ¾¾¾¾¾¾¾¾¾¾
5
NT50 = -1.655
Antilog. 1.655 = 1 : 45 (dilusyon)
Görüldüğü üzere Kaerber yönteminde de sonuç aynı çıkmaktadır.
Önemli not: Virusun 250 DKİD50 / 0.1 ml.de sabit dilusyonlarının yapılabilmesi için virusun hücre kültürlerindeki infektif %50 titresinin iyi bilinmesi gereklidir. Virusun titresi 10-6.833 ise, bu virus 10-3.833 dilusyonunda 0.1 ml miktarında 1000 tane 250 DKİD50 sahiptir. Eğer bu sulandırmadan 0.5 ml. alınıp üzerine 1.5 ml. buffer sol.konursa, oluşan karışımın 0.1 ml.'de 250 DKİD50 bulunmuş olur.
Eğer ikinci yöntem kullanılmak istenirse, yani, virus sulandırılır ve serum sabit tutulursa, test sonunda Nötralizasyon İndeksi, (Nİ) hesaplanır.
Nötralizasyon indeksi (Nİ50), virusun negatif serumla hücrelerde gösterdiği %50 infektif titreden, test serumları ile birlikte hücrelerde gösterdiği %50 infektif titrenin çıkarılmasından, elde edilir (aradaki farktır). Örn, virusun negatif (kontrol) serumla oluşan %50 infektif titresi 10-7.000 olsun, bir test serumu ile olan titresi de 10-4.000 olsun. Burada, Nİ50 = -7.000 - (-4.000)= -3.000 dür. Bu örnekte, bu test serumu 0.1 ml.inde virusun 1000 DKİD50 sini nötralize etmiştir.
Bu yöntemde de, serumları negatif, şüpheli ve pozitif olarak değerlendirebilmek için, iyi bir (güvenilir) negatiflik kriterinin saptanması ve buna göre karşılaştırılması gerekir.
Nötralizasyon testleri hücreler üzerinde yapılabildiği gibi, plaklara göre (plak nötralizasyon testi PNT), plak redüksiyon testi (PRT), plak supresyon testi (PST), plak inhibisyon testi (PİT); metabolik aktiviteye göre metabolik inhibisyon testi, MİT); hemadsorbsiyon testi (HAT), interferens inhibisyon testi (İİT) ve ayrıca embriyolu yumurtalarda ve deneme hayvanlarında da nötralizasyon testleri yapılabilir.
[1] Kaynak : Temel Mikrobiyoloji