Prof. Dr. Mustafa Arda
Ankara Üniversitesi Veteriner Fakültesi
Temel Mikrobiyoloji 1
01. Genel Bilgiler
02. Hücre Membranına Bağlanma (Adsorbsiyon)
03. Hücreye Giriş (Penetrasyon, Endositozis, İnternalizasyon)
03.01. Zarfsız Viruslar
03.02. Zarflı Viruslar
04. Kapsidin veya Zarfın Çıkarılması
05. Viral Ekspresyon
05.01. Transkripsiyon
05.02. DNA Viruslarında Transkripsiyon
05.03. RNA Viruslarında Transkripsiyon
05.04. Translasyon
05.05. Erken Proteinler
05.06. Geç Proteinler
06. Nukleik Asitlerin Replikasyonları (Genom Replikasyonu)
06.01. DNA Viruslarında Replikasyon
06.02. RNA Viruslarında Replikasyon
07. Viral Komponentlerin Sentezleri Ve Birleştirilmesi (Asamble)
07.01. İkosahedral (kübik simetri) Viruslarda
07.02. Helikal Simetrili Viruslarda
07.03. Kompleks Yapılı Viruslarda
08. Virusların Olgunlaşması (Maturasyon)
09. Virusların Hücrelerden Çıkışları (Serbest Kalma)
09.01. Hücrelerin Ölmesi (Sitolizis)
09.02. Tomurcuklanma
09.03. Ekzositozis
01. Genel Bilgiler
Virusların hücre içindeki multiplikasyon tarzlarını incelemede bakteriyofajların modelliğinden fazlaca yararlanılmıştır. Fajların bu özelliklerini saptamada kullanılan teknikler, hayvan viruslarına da adapte edilerek bunların canlı sistemlerde (hücre, embriyolu yumurtalar, deneme hayvanları) replikasyon aşamaları (virusların hücrelere bağlanılışından olgunlaşıp çıkıncaya kadar geçirdiği evreler) ayrıntılı olarak belirlenmiştir. Ancak, yine de tam olarak saptanamayan ve kesin olarak ortaya konamayan bazı noktalar hala bulunmaktadır. Elektron mikroskopların da virusların bu karakterlerini incelemede çok büyük faydaları olmuştur.
Virusların duyarlı hücrelerde replikasyon aşamaları, genellikle, 7 kısımda incelenmektedir. Her ne kadar, basamakların tümü direkt olarak ve gerçek anlamda nukleik asit sentezi ile bağlantılı değilse de, bu basamakların birlikte öğrenilmesinin konunun bütünlüğünün korunmasına ve daha kolay kavranılmasına yardımcı olacaktır. Bu aşamalar da,
1) Hücre membranına bağlanma (adsorbsiyon)
2) Hücreye giriş (penetrasyon, endositozis, internalizasyon)
3) Kapsidin ve/veya zarfın çıkarılması
4) Viral ekspresyon
a) Transkripsiyon
b) Translasyon
5) Nukleik asit sentezi (genom replikasyonu)
6) Viral komponentlerinin sentezi ve montajı (asamble)
7) Virusların olgunlaşması ve hücrelerden çıkışları
02. Hücre Membranına Bağlanma (Adsorbsiyon)
Virusların hücrelere girebilmesi ve bunun sonucunda da infeksiyon (litik veya nonlitik) oluşturabilmesi için, önce duyarlı hücrelere bağlanmaları gerekir. Zarfsız viruslarda kapsidin spesifik protein yapısı veya zarflı viruslarda, zarfın yüzeyinde bulunan protein ve glikoprotein karakterindeki özel moleküllerin (ligand, viral bağlanma proteinleri), duyarlı hücrelerin yüzeylerinde bulunan ve değişik kimyasal (protein, glikoprotein, oligosakkarid, lipoprotein, vs) yapıya sahip spesifik reseptörlere sıkıca bağlanması giriş için ilk ve önemli sinyali verir. Glikoproteinler, karbonhidratlardan daha fazla bağlanma etkinliğine sahiptirler ve daha fazla spesifiktirler. Aksi halde virionun ve hücre yüzeyinin negatif yüklü olmaları bağlanmayı (ligand-reseptör afinitesi) zorlaştırır. Bu nedenle virion ile hücre arasında kuvvetli bir kimyasal ilişkinin bulunması gereklidir. Ancak, şunu da hatırdan çıkarmamak gerekir ki, konakçının genetik duyarlılığı yanı sıra, kanlarında spesifik nötralizan antikorların da bulunmaması çok önemlidir. Ayrıca, konakçının immun yetmezlik hastalığına sahip olması veya immunsupresif ilaç kullanması infeksiyonu kolaylaştırır.
Yüzeylerinde spesifik reseptörler taşımayan hücreler, genellikle, viruslarla bağlanamazlar. Belli spesifik bir virusa duyarsız olan veya yüzeylerinde spesifik reseptör taşımayan hayvanlar, embriyolarına, spesifik reseptör geni verilerek transgenik hale getirilirse, bunların hücrelerinin yüzeylerinde spesifik reseptörler oluşur ve virus adsorbe olur ve içeri girebilir. Ancak, yüzeylerinde spesifik reseptör saptanamamasına karşın virusa duyarlı hücrelerin olabilmesi de mümkündür. Bu durum, viral genetik materyallerinin transfeksiyonla hücrelere girebileceği veya virusun primer reseptörlerden ayrı olarak, sekonder veya alternatif reseptörler de kullanabileceği anlaşılmıştır. Diğer bir ifade ile viruslar, bir veya birden fazla reseptörden yararlanmaktadırlar.
Bazı Viruslarda ligand ve reseptörleri
Virus | Ligand | Hedef hücre | Reseptör |
Pseudorabises virusu Vaccinia virusu Rhinovirus PPEV Coronavirus Rabies virus Parainfluenza virusu Influenza A Rotavirus Reovirus Fi DV Gibbon leukemia virusu | glll EGF VP, 1,2,3 VP 4 HE glikoprotein Glikoprotein H-N glikoprotein Hemaglutinin VP 7 Hemaglutinin (sigma 1) gp 120 gp 70 | Çeşitli hücre tipleri Çeşitli hücre Nasal epitel Intesnel epitel Çeşitli hücre tipleri Nöron Solunum epiteli Solunum epiteli Intestinel epitel T hücre, nöron T hücre,makrofaj Lenfosit | Heparan sulfat proteoglikan EGFR ICAM-1 IgG superfamilyası CEA’lerin glikoproteinleri ACR Glikoprotein(sialik asit içeren) “ “ “ “ B-AR ?CD4 Permeaz |
Fener,1993
EGF : Epidermal growth factor,
EGFR : Epidermal growth factor reseptörü
CEA : Carcinoembriyonic antigen
ACR : Acetyl cholinesterase reseptörü
B-AR : Beta adrenergic reseptör
ICAM-1 : Intracelluler adhesion molekülü-1
FIDV : Feline immundeficiency virus
PPEV :Porcine polioencephalomyelitis virusu
Bazı viruslar için, hücre yüzeyindeki reseptörlerin sayısının 100000'den fazla olabileceği belirtilmiştir. Örn, adenoviruslar için böyle bir durum söz konusudur.
Bir konakçının bütün hücreleri aynı virusa karşı tam bir duyarlılık göstermeyebilir veya bazı hücreler daha fazla hassas olabilirler. Örn, insanlarda poliovirusuna karşı nazofarinks, barsak, spinal kord (anterior kısım) hücreleri spesifik reseptörleri taşır ve virus bunlara bağlanır. Kuduz virusu için de nöronlar (asetil kolin reseptörleri) bağlanma yerlerini oluştururlar.
Viruslar ile reseptörler arasındaki ligand-reseptör ilişkisinin, hem virusun duyarlı hücreyi bulmada ve hem de doku tropizmini ve konakcı spesifitesini oluşturmada önemli fonksiyonu bulunmaktadır. Buna bağlı olarak, insanlarda infeksiyon oluşturan bazı viruslar (polio, kızamık, Kabakulak, HIV, vs) hayvanlarda ve hayvanlarda hastalık oluşturan bazı viruslar da (At vebası, sığır vebası, Marek, Gumboro, vs) insanlarda infeksiyon oluşturmazlar. Buna karşın kuduz virusu, Newcastle virusu ve bazı viruslar da zoonotik bir özellik gösterirler. Bu son durum, bir virusa karşı çeşitli hayvan türleri hücreleri yüzeyinde ortak reseptörlerin bulunmasından veya bir virus türü için, primer reseptörlerden ayrı oyarak sekonder veya alternatif reseptörlerin bulunmasından kaynaklanmaktadır. Örn, HIV için birden fazla türde reseptörün varlığı gibi. HIV'in esas reseptörü, lenfositlerin yüzeyindeki CD4 molekülüdür. Ayrıca nöronal hücre yüzeyinde de sekonder reseptörü vardır. Bazen de, bir reseptör birbirine yakın veya ayrı viruslar için ortak bağlanma yerlerini oluşturabilirler. Veya birbirine yakın viruslar (insan ve fare coronavirusları) farklı reseptörleri tercih edebilirler. Ayrı familyalarda bulunan viruslar aynı reseptörü kullanabilirler. Şöyle ki, Coxsackie B3 virusu (RNA, enterovirus) ile adenovirus-2 (DNA) aynı reseptörü paylaşılabilir. HIV (RNA, retrovirus) ile herpesvirus 7 (DNA), her ikisi de CD4'ü kullanabilirler. Bazen de viruslar, ikincil reseptörlere adapte olabilir ve bunlardan yararlanabilirler (swine vesicüler hastalığı virusu, SVDV).
Eğer hücre yüzeyindeki spesifik reseptörler enzimatik olarak giderilirse virusun bağlanamaması nedeniyle infeksiyon oluşmaz. Ancak, Coxsackie A9 (CAV-9, insan enterovirus) bir integrin olan vibronektin aVB3'ü reseptör olarak tercih eder. Bu integrin enzimatik olarak giderildiğinde virusun infeksiyonuna mani olunamamaktadır. Çünkü, virus bu reseptör yerine alternatif bir reseptörden yararlanmaktadır.
Tablo: Bazı viruslar için plasma membran molekülleri (reseptörler)
Reseptörler | Virus türleri ve familyaları |
| |
İmmunglobulin Benzeri | |
Moleküller | EMC-D (Picornaviridae) |
VCAM-1 | Major grup HRV, CAV |
ICAM-1(ilk ilmek) | 13, 18, 21 (Picornaviridae) |
| Poliovirus (Picornaviridae) |
PVR (ilk ilmek) | HIV-1,2; SIV (Lentiviridae) |
CD4 (ilk ilmek) | Human herpesvirus 7 |
| Fare hepatitis virusu |
CEA (çeşitli türleri, ilk ilmek) | (Coronaviridae) |
| Semliki Forest virus? |
MHC-1 | (Togaviridae) |
| Fare cytomegalovirus |
| (Herpesviridae) SV40 |
| Visna virus (Lentiviridae) |
MHC-II | |
İntegrinler | |
VLA-2 (alfa-zincir) | ECHO virus 1,8 (Picornaviridae) |
? (RGD-bağlayap protein) | FMDV (Picornaviridae) |
avB3 (vibronektin) | CAV 9, ECHO virus 22 (?) |
| (Picornaviridae) |
Transport Proteinleri | |
Fosfat taşıyıcı analog | Gibbon ape leukemia virus |
| (Retroviridae) |
| Amfotropik murin leukemia |
| virus (Retroviridae) |
Katiyonik amino asit | Ektotropik murin leukemia virus |
taşıyıcılar | (Retroviridae) |
Sinyal Reseptörleri | |
LDL reseptör protein grubu | Minor grup HRV'ler |
| (Picornaviridae) |
| Subgrup A avian leukosis ve |
| sarkoma virus (familya ?) |
Asetilkolin reseptör (a-1) | Rabies virus (Rhabdoviridae) |
EGF reseptör | Vaccinia virus (Poxviridae) |
Leukosit diferensiasyon | FIDV (Lentiviridae) |
antijeni (CD9) | |
Diğerleri | |
Aminopeptidase N | Human corona virus 229E |
| (Coronaviridae) |
| TGEV (Coronaviridae) |
Komplement reseptör (CR2) | EBV (Herpesviridae) |
Yüksek affiniteli laminin | Sindbis virus (Togaviridae) |
reseptör | |
Decay - accelerating factor | ECHO virus 7 (6,11,12,20,21 ?) |
(CD 55) | |
Membran kofaktör protein | Kızamık virusu (Morbiliviridae) |
Moesin | Kızamık virusu (Morbiliviridae) |
Glikoforin A | EMCV (Picornaviridae) |
| Reovirus (Reoviridae) |
Glaktosilseramid | HIV-1 (Lentiviridae) |
Eritrosit P antijeni | Parvoviridae B19 (Parvoviridae) |
BLVRcp | Bovine leukemia virus |
| (Retroviridae) |
Sialoglikoprotein GP-2 | Sendai virus (paramyxoviridae) |
Sialik asit | Influenza virus |
| (Orthomyxoviridae) |
| Reoviruslar (Reoviridae) |
| Grup A porcine rotavirus |
| (Rotaviridae) |
| Human coronavirus OC43, bovine |
| coronavirus (Coronaviridae) |
Heparan sulfat | Human CMV (Herpesviridae) |
| HSV |
Wimmer.1994;Levy, 1994 |
VCAM : Vascular cell adhesion molecule |
ICAM : Intra cellular adhesion molecula |
PVR : Poliovirus reseptörü |
CEA : Carcinoembriyonic antigene |
EMCV : Encephalomyocarditis virus |
CAV : Cosackievirus |
TGEV : Transmissible gastroenteritis virusu |
EBV : Epstein Barr virusu |
HIV : Human immunodeficiency virus, |
MHC : Major histocompatability complex, |
HRV : Human rhinovirus |
HSV : Herpes simplex virus |
FIDV : Feline immunodeficiency virus |
Yukarıda açıklanan nedenlerle viruslar birden fazla ve farklı yapıda reseptör kullanabilmektedirler.
Zarflı viruslar için hücre yüzeyindeki reseptör sayısının, zarfsız olanlardan, daha fazla olduğu belirtilmiştir. Bu durum da, zarflı virusların daha kolay hücrelere girebileceğini ve infeksiyon oluşturabileceğini de göstermektedir.
Viruslar, hücre yüzeyindeki reseptörlerle, ilk başlangıçta zayıf kuvvetlerle (hidrojen bağları, iyonik atraksiyon, van der Waals kuvvetleri) bağlanır. Ayrınca, virusun tek bir reseptöre bağlanması da adhezyonu reversible duruma getirir. Zamanla, bir kaç reseptörle ilişki kurması, bağlantıyı güçlendirir ve irreversible hale koyar. Bu nedenle kros bağlantılar adhezyonu kuvvetlendirirler. Bu fenomene, aynı zamanda, ortamın pH'sı ve tuz yoğunluğunun da etkisi bulunmaktadır. Ayrıca, reseptörlerde ve/veya ligandlarda bulunan amino ve karboksil gruplarının da rolleri vardır. Çünkü, bu grupların tahribi veya inaktive edilmesi bağlanma üzerine olumsuz etkilediği açıklanmıştır. İnsan rhinovirus tip-2 ile poliovirus tip-2'nin hücrelere bağlanması Con A (lektin, concanavalin A) tarafından önlenebilmektedir. Con A, reseptörlerdeki alfa-D-mannoz molekülleri ile ilişki kurarak bunların aktivitesini önler ve bağlanmayı inhibe eder.
Virusların yüzeylerinde bulunan bağlanma molekülleri (ligand), hücrelerdeki birkaç tür reseptörle bağlantı kurabilecek bir karakter taşımaktadırlar. Zarflı viruslarda zarfta bulunan peplomerler (hemaglutinin, neuraminidase, F-proteini) ile adenoviruslarındaki fiberler reseptörlere bağlanmada etkin rol oynarlar. Paramyxoviruslarında virionun yüzeyindeki F-proteini, hücre yüzeyinde enzimatik olarak aktive olduktan sonra, sitoplasmik membranla birleşir (füsyon). Böylece serbest kalan nukleokapsid sitoplasmaya transfer edilir,. Reseptörler, sadece virusları bağlamada etkinlik göstermez, aynı zamanda virusun sitoplasmaya geçişine ve hücreye çeşitli uyarımları vermede de etkili olmaktadır. Ancak, bazı reseptörlerin de, virusu sadece adsorbe ettiği buna karşın hücre içine girmede etkisinin olmadığı da açıklanmıştır. Örn, HIV'in rodent hücrelerindeki CD4'e bağlandığı fakat internalizasyona yardımcı olmadığı belirtilmiştir.
Viruslar, yukarıda açıklanan ligand-reseptör bağlantısı nedeniyle hücrelere adsorbsiyonu (direkt mekanizmalar) yanı sıra, indirekt mekanizmalar yardımı ile de hücrelere bağlanabilir ve internalize olabilir. Bu son durumda, kanda bulunan spesifik antikorların (özellikle, İgG ve İgM) ve komplementin rolleri fazla olmaktadır. Hücrelere bağlanmada reseptör olarak FcR ve CR (komplement reseptörü) fonksiyoneldir. Viruslara, Fab bölgeleriyle bağlanan antikorların serbest kalan Fc porsiyonları hücre yüzeyindeki FcR'leri ile de kolayca bağlanır. Oluşan, virus + antikor + FcR veya CR kompleksi, ayrıca, hücre içine sinyal vermede, virusun internalizasyonunda ve infeksiyonunda (antikora bağımlı infeksiyon, ABİ) görev alabilir. Bu son durum, antikorların varlığında, virusların da infeksiyon yapabileceklerini, immun bireylerden elde edilen hücrelerde viral değişikliklerin oluşabileceğini, virusların hücrelerde intrasellüler olarak canlı kalabileceklerini ve infeksiyon oluşturabileceği gibi önemli sorunları da beraber getirmektedir.
03. Hücreye Giriş (Penetrasyon, Endositozis, İnternalizasyon)
Elektron mikroskopik ve diğer, in vivo ve in vitro çalışmalar, virusların hücrelere girişlerinde oldukça ayrıntılı bilgiler vermiştir. Virusların hücrelerdeki spesifik reseptörlere sıkıca bağlanması ve bu fenomenin irreversible olması, hücreye giriş için ilk adımı oluşturmasına karşın, bu kuvvetli ilişkinin devam etmemesi, virusun serbest kalmasını önlememesi ve girişe engel olmaması yönlerinden de önemlidir. Virus, hücre yüzeyine adsorbe olduktan sonra peplomerlerdeki glikoproteinlerde bazı konformasyonal değişiklikler meydana gelir ve bunlar virusun girmesine yardımcı olur. Zarflı viruslardaki F-proteinin, sitoplasmik membranla birleşmesi (füsyon) nukleokapsidin sitoplasmaya geçişini çok kolaylaştırır. Zarfta bulunan neuraminidase enzimi (sialidase), reseptör proteinlerdeki sialik asiti hidrolize ederek virusun serbest kalmasına (elüsyon) ve içeri girişine yardımcı olur. Endositozis (viropeksiz) olayı da, hücrelere girişte yardımcı olan bir fenomendir. Reseptörler, viruslarla bağlanmaları yanı sıra, virusun içeri girmesine ve iç kısma sinyal vermede de görev yaparlar. Bu sinyaller, virus sitoplasmaya geçmeden önce, hücre içinde virus için bir hazırlık yapılmasını da uyarır.
Viruslar zarfsız ve zarflı olduklarına göre başlıca 3 genel mekanizma ile sitoplasmik membranı geçerek sitosola ulaşırlar.
Virusların hücrelere giriş tarzları yandaki şekilde gösterilmektedir. | 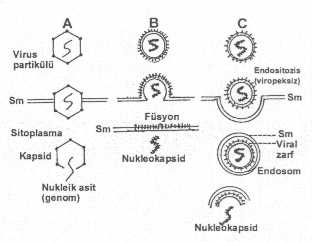
|
03.01. Zarfsız Viruslar
Adenoviruslar, reoviruslar ve diğer zarfsız viruslar da nukleokapsidlerinde meydana gelen bazı değişiklikler aracılığı ile sitoplasmik membranı kolayca geçebilir (kapsid ile birlikte) sitoplasmaya ulaşır ve burada kapsidleri enzimatik olarak ayrıştırılarak nukleik asitler serbest kalırlar.
03.02. Zarflı Viruslar
Zarflı viruslar da başlıca iki tarzda sitoplasmik membranı aşarak hücre içine girerler.
1) Plasma membranı ile füsyon: Yüzeyinde F-proteini bulunan viruslarda, bu protein hücre membranı ile kolayca birleşir ve nukleokapsid serbest kalarak sitoplasmaya ulaşır. Bu olguda,. zarf hücre membranı ile birlikte dışarıda kalır içeri girmez (paramyxovirusları ve diğerleri)
2) Endositozis (viropeksiz): Endositozis, normal hücreler tarafından uygulanan, hücre yüzeyindeki reseptörlere bağlanmış olan partiküllerin internalizasyon yöntemidir. Viruslar hücre yüzeyindeki reseptörlere tutunduktan sonra, virusu tümden saran plasma membranı ile çevrilir ve böylece içeri alınır. Bu olguda, virionun etrafında zarftan ayrı olarak sitoplasmik membrandan da bir katman bulunur. Virionun etrafındaki dış muhafaza çıkarıldıktan sonra endosomla birleşirler (asidik lisozomal vesiküller). Burada, asidifikasyonun etkisi ile zarftan da sıyrılarak nukleokapsid sitosola geçer. Togaviruslar, orthomyxoviruslar, rhabdoviruslar ve diğer helikal simetrili viruslarda bu tarz girişe rastlanmaktadır.
Zarflı ikosahedral viruslarda (flaviviruslar, hepadnaviruslar) bu iki mekanizmadan birisinden yararlanmaktadırlar. Ya zarf dışarıda kalır kapsid direkt olarak içeri girer veya virus tümden endositozisle içeri alınır. Sonra muhafazalarından sıyrılarak viral genom serbest kalır.
İndirekt mekanizma: Yukarıda bahsedilen ve virusların direkt olarak hücrelere genel giriş mekanizmaları yanı sıra indirekt mekanizmaları kullanarak internalizasyonu üzerinde gerek in vivo ve gerekse in vitro bir çok araştırmalar yapılmış ve yayımlanmıştır. İndirekt mekanizmada, virus yüzeyindeki moleküller yanı sıra, bivalent ligandların (antikorlar) ve hücre yüzeyinde bulunan özel reseptörlerin (FcR ve CR) önemleri bulunmaktadır. Ligandlar arasında İgG (İgG1, İgG3); farelerde İgG2a; İgG + komplement; İgM + komplement), komplement, soluble CD4 gibi moleküller yer almaktadır. Monositler, makrofajlar, polimorfnukleer hücreler, dendritik hücreler (Langerhans hücreleri), B-, T-, NK hücreleri FcR ve CR yönünden oldukça zengindirler. İgG için 3 tür FcR (FcRI, FcRII, FcRIII), İgM, İgA ve İgE için de birer tür reseptör bulunur. FcR'lere aynı zamanda intestinal hücrelerde de rastlanılmaktadır. Fare makrofajlarında da 3 tür FcR (FcRI, FcRII, FcRIII) vardır ve bunlar sıra ile İgG2a, igG2b ve İgG3'e bağlanırlar. Bivalent ligandların hem viruslara ve hem de hücre yüzeyindeki reseptörlere bağlanması sonucu da oluşan (virus+ligand+reseptör) kompleksinin internalize olabileceği ve hücreleri infekte edebileceği araştırıcılar tarafından açıklanmıştır. Antikor olmadan da (non immunolojik olarak), virus + komplement + faktör B kompleksinin komplementi indirekt yoldan aktive ederek infeksiyonu restore ettiği HIV-1 ile infekte MT-2 hücrelerinde yapılan in vitro çalışmalarda ortaya konulmuştur. Yüzeylerinde FcR taşımayan hücrelerde, C3R'nin var olması durumunda, İgG+komplement+virus kompleksinin infeksiyonu kolaylaştırabileceği belirtilmiştir.
Monoklonal veya poliklonal nötralizan antikorların, eğer nötralizan antikorlar nötralizasyon sınırının üstündeki sulandırılmalarda ise, antikora bağımlı infeksiyonu desteklediği belirtilmiştir. Genellikle, pozitif serumların yoğun konsantrasyonları virusları nötralize etmelerine karşın yüksek sulandırmalarda virusun üremesini destekleyici etkiye sahip olabilmektedirler. Özet olarak, indirekt mekanizmaların da virusun hücreye girişine ve infeksiyonuna yardımcı olabileceği yapılan çalışmalarda ortaya konulmuştur. Eğer, kanda, antikorlar, nötralizasyon noktasının üzerinde bulunuyorsa, etkili olabilmekte ve virusun hücreye girişini ve infeksiyon oluşturmasını desteklemektedir (antikora bağımlı infeksiyon).
04. Kapsidin veya Zarfın Çıkarılması
Viral genom sitoplasmaya girdikten sonra hücre içindeki çeşitli enzimlere (DNase, RNase, protease, vs) çok duyarlı olduğundan, hemen transkripsiyonun ve diğer işlemlerin (translasyon, replikasyon) başlaması ve bitirilmesi gerekmektedir.
Virusların yapısal karakterlerine göre başlıca dört tür mekanizma ile kapsid ve/veya zarflardan kurtulma gerçekleştirilmektedir. Bunlar da,
1) Zarfsız viruslarda (picornavirusları gibi), virion hücre membranına bağlandıktan sonra, kapsidde konformasyonal değişiklikler meydana gelerek kapsid proteinlerinden VP2 ve VP4'lerde serbest kalma ve kayıplar meydana gelir. Bu durum, kapsidin proteazlara daha duyarlı hale gelmesine neden olur. Plasma membranında oluşan zayıf noktalardan nukleokapsid sitoplasmaya ulaşır ve burada kapsidden ayrılan genom (nukleik asit) fonksiyonu olan bölgeye gider.
2) Herpesviruslarında nukleokapsid sitoplasmaya girdikten sonra nükleer membranla birleşir ve DNA nükleer membrandaki deliklerden içeri girerek replikasyon bölgesine ulaşır.
3) Poxviruslarında, nukleik asitin etrafındaki zarflardan ayrılma, sitoplasmadaki endosomlar (veya vakuoller) içinde gerçekleşir ve DNA serbest kalarak sitoplasmaya geçer ve replikasyonun bütün aşamaları sitoplasmada tamamlanır.
4) Zarflarında F-(füsyon) Proteini bulunan viruslarda (paramyxoviruslar, vs) bu spesifik protein hücre membranı ile birleşerek membranda kalır ve nukleokapsid serbest kalarak sitoplasmaya geçer ve buradan replikasyon bölgesine gelir. Diğer zarflı viruslar (orthomyxovirus, togavirus, vs) ise endositozis (viropeksis) ile içeri girer, endosomlar içinde toplanır ve burada zarflarından ayrılan genom serbest kalarak sitoplasmaya geçer.
Helikal nukleokapside sahip viruslarda transkripsiyon, viral RNA henüz zarftan tam ayrılmadan önce başlar. İkosahedral zarfsız reoviruslarında ise, sadece bazı kapsid proteinleri çıkartılır ve serbest kalan viral genom bütün fonksiyonları sürdürür. Hatta, viral genom kapsidden tam ayrılmadığı zaman bile transkripsiyon başlayabilir.
05. Viral Ekspresyon
Viral genomun ekspresyonu başlıca iki önemli aşamada gerçekleşmektedir. Bunlarda, 1) Nukleik asitlerin transkripsiyonu ve 2) Translasyonudur. Ancak, henüz bütün virus familyalarının veya virusların viral ekspresyonlarının ayrıntılı aşamaları tam belirlenmiş değildir.
05.01. Transkripsiyon
Virusların ekspresyonlarının ilk ve önemli aşamasını mRNA (mesenger RNA) sentezi oluşturur (transkripsiyon). Viral genom tarafından spesifiye edilen mRNA'lar, aynı zamanda, sellüler ribosomlarda viral proteinlerin sentezini de (translasyon) programlar. Viral nukleik asitler, virusların strüktürel proteinleri yanı sıra, nukleik asit replikasyonu, gen ekspresyonu, virusun asamblesi, olgunlaşması ve hücrelerden çıkışları için gerekli olan özel ve çok spesialize olmuş proteinlerin ve enzimlerin sentezlerini de yönetir. Diğer bir ifade ile viruslar, duyarlı hücrelerin sitoplasmalarına girdikten ve etraflarındaki muhafazalardan (kapsid veya zarf) kurtarıldıktan sonra, konakcı hücrenin bütün olanaklarını, kendi üretimi için programlar ve kendi lehine çevirirler. İnfeksiyonun başlangıcında ve infekte hücrelerde, viral mRNA'nın meydana gelmesi, hücre yönetiminin virus tarafından ele geçirildiğini de ifade eder.
Transkripsiyon, genel anlamda, genomda (DNA viruslarında) kodlar (şifreler) halinde bulunan genetik bilgilerin (informasyonlar) DNA'ya bağımlı RNA polimeraz enziminin (transkriptaz) katalitik etkisi ile sentezlenen mRNA'ya yine şifreler halinde aktarılması olgusudur. Diğer bir ifade ile mRNA genetik şifrelerden oluşur.
Bakterilerde genetik materyalin çift iplikçikli, sirküler ve sarmal DNA olması nedeniyle, transkripsiyonda bu iplikçiklerin sadece biri (3'¬ 5' yönünde olanı) kullanılarak, transkriptaz enziminin RNA polimeraz enziminin polimerizasyon etkinliği ile bu iplikçikte (DNA) bulunan genetik bilgiler tek iplikçik mRNA'ya şifreler halinde aktarılır. Bakterilerde kolay olan bu fenomen, viruslarda ise çok daha komplikedir.
Viruslar, genetik materyal olarak DNA veya RNA'lardan sadece birine sahip olmaları, tek veya çift iplikçikli, lineer veya sirküler, pozitif veya negatif polariteli, segmentli veya segmentsiz bulunmaları transkripsiyon mekanizmalarına etkilemekte, bu durumlara bağlı olarak ta, transkripsiyon için değişik stratejilerin ortaya çıkmasına yol açmaktadır.
Ayrıca, ökaryotik hücrelerde RNA'ya bağımlı RNA polimeraz enzimi de bulunmamaktadır. Bu nedenle de ssRNA (single stranded RNA) ve dsRNA (double stranded RNA) virusları transkripsiyonları için bu enzimlerin kodlarını kendi genomlarında taşımak zorundadırlar. Bunun yanı sıra, ökaryotik hücreler ilk başlangıçta sentezlenen polisistronik mRNA'ları daha küçük proteinlere transle edebilecek mekanizmalara da sahip değildirler. Bu yönleri ile de, sentezlenen polisistronik mRNA'ların monosistronik hale getirilmesi gerekmektedir.
Virus gruplarının özelliklerine göre değişiklikler gösteren transkripsiyon stratejilerine ait aşağıda çok kısa ve özlü bilgiler verilmektedir.
05.02. DNA Viruslarında Transkripsiyon
Bazı DNA viruslarında, mRNA, hücreye ait, DNA'ya bağımlı RNA polimeraz enziminin (transkriptaz) katalitik etkisi ile sentezlenir (transkripsiyon). Poxviridae viruslarında ise viral transkriptaz enzimi kullanılır. Ancak, viral DNA'nın transkripsiyonu, nukleik asitte bulunan bütün genlerin aynı anda ve devamlı olarak ekspresyonunu sağlayacak tarzda proglanmış değildir. Şöyle ki, genomik DNA'da bulunan bazı genler erken ve bir kısmı da geç transkripte edilirler. DNA virusları, RNA viruslarının aksine, sellüler ayrıştırma mekanizmaları kullanarak, sentezlenen polisistronik RNA'ları monosistronik mRNA molekülleri haline dönüştürebilme kapasitesine sahiptirler. DNA virus familyaları arasında, viral veya sellüler transkriptazın kullanma durumuna ve replikasyon bölgesinin sitoplasma veya nukleus olduklarına göre, transkripsiyon mekanizmalarında da bazı spesifik değişiklikler meydana gelmektedir. Transkripsiyon ve replikasyon aşamaları, poxvirusları hariç, nukleusda gerçekleştirilir.
DNA viruslarında saptanan transkripsiyon stratejileri yandaki şekilde özet olarak gösterilmiştir. | 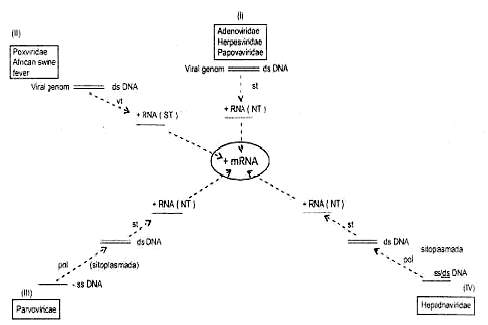 |
1) Çift iplikçikli DNA (dsDNA), sellüler transkriptaz kullananlarda: Adenovirusları, herpesvirusları ve papovaviruslarında, viral DNA'nın bir iplikçiği kullanılarak, konakcı hücrelerinin çekirdeklerinde hücreye ait ve DNA'ya bağımlı RNA polimeraz II enziminin katalitik etkisi ile transkripte edilir. Polisistronik ve fakat subgenomik (genlerin hepsini değil bir kısmını taşıyan) özellik gösteren bu transkriptler (+mRNA), enzimatik olarak ayrıştırılarak monosistronik mRNA'lara dönüştürülür. Bunlar nukleustan sitoplasmaya transfer edilerek ribosomlar üzerinde translasyona tabi tutulurlar (No.I).
2) Çift iplikçikli DNA (dsDNA), virion transkriptaz kullananlarda: Sitoplasma da replike olan viruslarda (poxvirusları, African swine fever virusu), viral genom, kendi transkripsiyonunu sağlamak için transkriptaz enziminin kodlarını taşır. Virus sitoplasmaya ulaşınca, muhafazalarında kurtulur ve serbest kalan genom, önce transkriptaz enziminin sentezini gerçekleştirir. Enzim, DNA'yı transkripte ederek monosistronik (+) mRNA'ların oluşmasına yol açar (No. II).
3) Tek iplikçikli DNA (ssDNA) sellüler transkriptaz kullananlarda: Parvoviruslarında genomik ssDNA, kalıp olarak kullanılarak, hücreye ait polimeraz enzimi tarafından çift iplikçikli (dsDNA) haline dönüştürülür. Bu DNA hücre nukleusuna girerek, burada, hücresel transkriptaz enzimi yardımı ile polisistronik mRNA sentezlenir. Bu da enzimatik olarak ayrıştırılarak monosistronik mRNA'lar elde edilir. Buradan sitoplasmaya transfer edilerek translasyonda kullanılırlar (No III).
4) Tek/çift iplikçikli DNA (ss/dsDNA), sellüler transkriptaz ve virion polimeraz kullananlarda: Hepadnaviruslarında, genomun bir kısmı tek iplikçiklidir. Bu tek iplikçik olan kısım viriona ait DNA pol enzimi yardımı ile çift iplikçik haline getirilir. Böylece tüm genom çift iplikçikli (dsDNA) olur. Viral genom nukleusa transfer edilerek burada, sellüler RNA pol II enzimi aracılığı ile dsDNA'nın değişik promotorlarından başlayan + mRNA'lar sentezlenirler (No. IV).
05.03. RNA Viruslarında Transkripsiyon
RNA Viruslarında transkripsiyon, DNA viruslarından daha komplikedir. Ökaryotik hücreler viral genomik RNA'dan, mRNA sentezi için, RNA'ya bağımlı RNA polimeraz enzimine sahip olmadıkları için, transkripsiyon da viral genomik RNA'ları kalıp olarak kullanamazlar. Bu nedenle de, RNA virusları (ssRNA ve dsRNA), kendi genomlarında, replikasyonları için gerekli olan enzimlerin kodlarını taşırlar (RNA'ya bağımlı RNA polimeraz enzimi).
Retroviruslar hariç tutulursa, diğer RNA virusların transkripsiyonları hücre sitoplasmasında gerçekleştirilir.
RNA viruslarının transkripsiyon stratejileri yandaki şekilde çok özet olarak gösterilmektedir. | 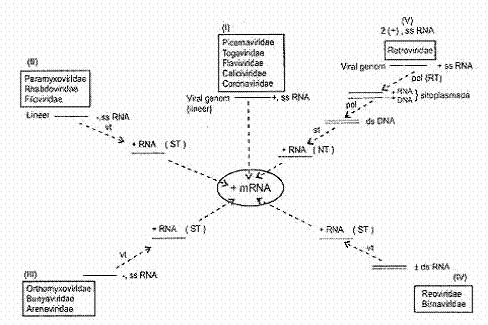 |
1) Pozitif polariteli, tek iplikçikli RNA (+, ssRNA) viruslarında: Picornaviridae, Togaviridae ve diğerlerinde, genomlar, mRNA ile aynı polaritede olduklarından hem infeksiyöz yeteneğe ve hem de mRNA aktivitesine sahiptirler. Bu nedenle de genomlarında kendilerinin transkripsiyonu için transkriptaz enziminin kodlarını taşımazlar. Viral genom doğrudan, ribosomlarda translasyona tabi tutulur (No.I).
2) Negatif polariteli, tek iplikçikli, virion transkriptazlı (-, ssRNA) viruslarında: Segmentsiz tek iplikçik RNA viruslarında, genom, kendini transkripte edebilmek için, RNA'ya bağımlı transkriptaz enziminin kodlarını taşırlar. Bu enzim, negatif polariteli genomik RNA'ları kalıp olarak kullanarak bunlardan pozitif polariteli RNA'ların sentezini katalize eder. Bunlar da mRNA aktivitesine sahiptirler (+ mRNA). (No.II).
3) Negatif polariteli, tek iplikçikli, virion transkriptazlı (-, ssRNA) viruslarında: Segmentli olan RNA viruslarında, her bir segment, virionda kodlanın transkriptaz enzimi yardımı ile transkripte edilir ve bunlardan pozitif polariteli RNA'lar oluşur. Bunlar da mRNA aktivitesi gösterirler ve ribosomlarda translasyona tabi olurlar (No.III).
4) Çift iplikçikli, virion transkriptazlı RNA (±, dsRNA) viruslarında: Segmentli ve çift iplikçikli olan birnaviruslar ve reoviruslarında, genomların negatif segmenti, viral transkriptaz enzimi yardımı ile transkripte olur ve bunlardan pozitif polariteli RNA'lar meydana gelir. Bunlar da mRNA etkinliğine sahiptirler (No.IV).
5) İki molekül tek iplikçikli RNA genoma sahip pozitif polariteli, virion transkriptazlı viruslarda (+2ss RNA): Retroviruslarında pozitif polariteli olan genom diploid (çift molekül) bir özellik taşır. Tek iplikçik viral genom, sitoplasmada, virionda kodlanan revers transkriptaz (RNA'ya bağımlı DNA polimeraz) enzimi tarafından komplementer DNA (cDNA) sentezlenerek hibrid bir molekül (RNA-DNA) oluşur. Sonrada bu, dsDNA haline getirilir (proviral DNA). Çift iplikçikli proviral DNA hücrenin çekirdeğine girerek kromozoma integre olur ve burada sellüler RNA polimeraz II tarafından transkripte edilerek + m RNA sentezlenir. Bu transkript, sitoplasmaya transfer edilir ve burada translasyona tabi tutulur (No.V).
05.04. Translasyon
Genel anlamı ile translasyon, mRNA'da şifreler halinde bulunan genetik bilgilerin (informasyonların) sitoplasmada ribosomlar üzerinde deşifre edilerek (çözülerek) proteinler haline dönüştürülmesi fenomenidir. Gen ekspresyonunun en önemli bir kısmını oluşturan translasyon komplike bir karakter taşır.
Prokaryotlarda (bakterilerde) transkripsiyonla sentezlenen tek iplikçik mRNA polisistronik (yani, bakterilerin m RNA'sı, genomda bulunan hemen bütün proteinlerin şifresini taşır, ve mRNA'nın 5'-terminusunda bir promotor ve 3'-terminusunda da terminasyon sekansları bulunur) bir karakter taşımasına karşın, ökaryotlarda monosistroniktir (her mRNA bir proteini kodlar ve her proteinin ayrı bir promotor ve terminatör sekansları vardır). Bakteriler ve gerekse ökaryotlar, kendi mRNA'larını, kendilerine ait olan translasyon mekanizmalarında kolayca deşifre edip protein haline çevirmesine karşın, virusların böyle mekanizmaları olmaması nedeniyle, viral genomda şifreler halinde (kodlanmış) bulunan proteinlerin deşifre edilebilmesi, ancak girdiği hücreler içinde ve hücrelerin ribosomlarında gerçekleşmektedir. Bu nedenle de virusların genom ekspresyonları (transkripsiyon ve translasyon) ve replikasyonları ayrı bir özellik taşımaktadır. Viruslar (hayvan virusları) bu amaçlar için ökaryotik hücrelerden yararlanırlar. Ökaryotiklerin translasyon mekanizmaları daha komplike bir durum gösterir ve monosistronik m RNA'ları kullanabilir. Viral m RNA'ların da, ökaryotik ribosomlarca kullanılabilmeleri, bunların monosistronik hale getirilmesi ile mümkündür. Diğer bir ifade ile, viral m RNA'ların ökaryotik ribosomların çalışma mekanizmasına uymaları ve bu mekanizmalarca algılanması gereklidir.
RNA virusları 3 farklı yol izleyerek monosistronik mRNA kuralına uyarlar. Bunlar da,
1) Segmentli genoma sahip viruslarda (orthomyxovirus, reoviruslar) her bir genomik segment bir gen karşılığı olarak kabul edilir ve her segmentin transkripsiyonu sonu oluşan m RNA'lar monosistronik bir özellik taşırlar.
2) Paramyxoviruslar, togaviruslar, rhabdoviruslar ve coronaviruslar, her genin ön kısmının (başlangıcındaki) transkripsiyonu sonu sentezlenen mRNA'lar monosistronik özelliktedirler.
3) Picornaviruslarında pozitif polariteli genomun 5'-terminusuna yakın kısmında tek bir ribosom bağlanma yeri bulunmaktadır. Bu bölüm transle edilerek uzun bir poli protein sentezlenir ve bu sonradan enzimatik olarak küçük proteinlere (monosistronik) ayrıştırılır.
Proses edilerek monosistronik bir duruma getirilmiş ve 5'-terminusu Cap'lı olan viral mRNA'lar, bu ucu ile 40 S'lik ribosomal alt üniteye bağlanırlar. Bu alt ünite, m RNA üzerinde başlatma kodonuna (AUG) gelinceye kadar hareket eder. Burada 60 S'lik büyük ribosomal alt ünite ile birleşir, bir başlatma kompleksi oluşturur ve hemen translasyon başlar.
Segmentli viruslarda her segment ayrı bir translasyona tabi tutulur.
05.05. Erken Proteinler
DNA viruslarında, mRNA'dan erken sentezlenen proteinler arasında, çeşitli aktiviteye sahip enzimler, viral genomun ekspresyonunu regule eden proteinler, sellüler protein sentezini ve sellüler nukleik asit sentezini suprese eden proteinler yer almaktadır.
05.06. Geç Proteinler
Geç viral proteinler, genellikle, hücre infeksiyonun ileri dönemlerinde ve viral replikasyondan sonra, mRNA'ların translasyonlarından elde edilirler. Geç proteinlerin çoğu, yapısal bir karakter taşırlar ve özellikle, regulatör fonksiyona sahip olanları, fazlaca sentezlenirler. Bunlar, erken viral genlerin veya hücresel genlerin transkripsiyon ve translasyonlarını regule ederler.
DNA viruslarında bazı proteinlerin sentezinin, sırasının ve miktarlarının düzenlenmesi (regulasyonu), genellikle, transkripsiyon aşamasında yapılır. RNA viruslarında da, yapısal olmayan proteinler erken ve yapısal olanlar da geç sentezlenirler. Sentezin kontrolü translasyon aşamasında yapılmasına karşın, DNA viruslarında olduğu gibi tüm düzenlilik göstermemektedir.
Caliciviruslarında, coronaviruslarında ve togaviruslarında pozitif polariteli viral RNA'nın 5'-terminusu (bu uç, non strüktürel proteinleri kodlar); erken translasyona tabi tutulur ve negatif sense (polariteli) RNA'nın sentezini başlatır. Bu da subgenomik RNA' nın transkripsiyonu için kalıp görevi yapar. Yapısal proteinler, genellikle, çok miktarda sentezlenirler.
Picornaviruslarında, caliciviruslarında ve togaviruslarında polisistronik mRNA'lardan sentezlenen poli proteinler, enzimatik olarak belli bölgelerinden ayrıştırılarak fonksiyonel proteinler haline getirilirler (posttranslasyonal modifikasyon).
Hücre içinde sentezlenen proteinler translasyon ve replikasyondaki fonksiyonlarına göre gerekli olan yerlerine giderek reaksiyonların tam ve zamanında yapılmasını sağlarlar. Ancak, bu migrasyonu etkin ve zamanında kontrol eden mekanizmalar tam olarak aydınlatılmış değildir. Hücre içindeki yer değiştirmede sitoskeletonların rolü büyüktür.
Aşağıdaki tabloda viral genom tarafından kodlanan başlıca proteinler gösterilmektedir.

06. Nukleik Asitlerin Replikasyonları (Genom Replikasyonu)
Virusların genom replikasyonları, genel hatları ile, bakterilerinkine benzerse de, viral genomun, DNA veya RNA olması, çift veya tek iplikçikli, segmentli-segmentsiz, lineer-sirküler bir özellik taşıması nedeniyle bazı farklılıklar taşımaktadırlar. Bu durum viruslar arasında değişik stratejilerin meydana gelmesine ve uygulanmasına yol açmıştır.
06.01. DNA Viruslarında Replikasyon
DNA virus familyalarının her birinde ayrı bir replikasyon mekanizması uygulanmaktadır. DNA virusları replikasyonları için gerekli olan proteinleri, enzimleri ve diğer makromolekülleri, replikasyon başlamadan önce hücre içinde hazır olarak ve yeterince bulmaları gereklidir. Bu proteinler viral ve/veya hücre orijinlidirler. Hücrelerce sağlananlar, ancak hücrelerin belli zamanlarında (S fazı, DNA sentez fazı) gerçekleşmektedir. Bu nedenle de, virusların replikasyon sırasında hücrelerin S fazına bağlılıkları önemlidir. Ancak, bu durum viruslar arasında da değişiklik gösterir. Şöyle ki, küçük viruslardan olan parvovirusları, infekte ettikleri hücrelerin DNA'ları replike olurken, viral DNA'da aynı anda replike olmaya başlar. Bu yönden, hücrelerin S-fazı bu viruslar için önem taşır. Buna karşın, büyük virusların sellüler fonksiyona ve proteinlerine bağımlılığı daha azdır. Çiçek virusları sitoplasmada replike olduklarından, hücrelerin S-fazına olan gereksinimleri daha sınırlıdır. Ayrıca, viral genom, hücre sitoplasmasında replikasyonu sağlayacak bazı gerekli enzimlerin kodlarına da sahiptirler. Diğer DNA viruslarının da hücre (konakcı) replikasyon mekanizmalarına olan bağımlılıkları değişiklik göstermektedir. Parvoviruslar ve papovaviruslar replikasyonları için, konakçının DNA' sını bağımlı DNA polimeraz enzimini kullanmasına karşın büyük viruslardan olan adenoviruslar, herpes viruslar ve poxvirusları polimeraz enzimini kendi genomlarında şifreler halinde taşırlar. Viral polimeraz, hücre polimerazından daha hızlı aktiviteye sahip olmasına karşın, daha az spesifiktir. Bu sebeple, viral enzim daha fazla mutasyonlara yol açtığı gibi antiviral ilaçlar için de hedef bölge oluştururlar.
Viruslar, her zaman, S-fazındaki hücreleri bulamayabilirler. Bu nedenle, bazı viruslar, kodladıkları özel proteinlerle hücreleri aktive ederek S-fazına geçmelerini uyarabilmektedirler.
Replikasyonda çok gerekli olan DNA polimeraz enzimi, viral iplikçikte primer moleküller olmadan polimerazisyona başlatamaz. Bu enzim ancak, primerlerin varlığında DNA'ın 3'-terminusuna (3' -OH ucuna) nukleotidleri ekleyebilir ve polimerazisyonu sürdürebilir. Bakterilerde primerler genellikle, primaz enzimi tarafından sentezlenen kısa (50-100 nukleotid) RNA karakterindeki tek iplikçik oligonukleotidlerden oluşmaktadır. Viruslar bu sorunu aşabilmek için değişik stratejiler kullanırlar. Bazılarında 5'-terminusta bulunan protein molekülü, bir kısmında ise genomda oluşan çengel tarzdaki kıvrılma veya komplementer uçlar replikasyon için başlangıç yerlerini oluşturarak polimeraz enziminin bağlanmasına ve polimerizasyonuna yardımcı olurlar.
Replikasyonda diğer önemli sorun da, genomun sarmal ve süpersarmal yapısının replikasyon sırasında önceden çözülerek replikasyona hazır bir duruma getirilmesidir. Bunun için helikaz enzimlerinden yararlanılır. ATPase aktivitesi olan bu enzim, replikasyonun önünde giderek DNA'yı açar (çift iplikçikli DNA) ve açılan iplikçikleri de SSBP (single stranded binding protein) olarak tanımlanan proteinler tarafından açık tutulması sağlanarak polimerizasyon sürdürülür.
DNA polimeraz enzimi replikasyon çatalında, açılan parental iplikçiklerinden tersine (polimeraz enziminin aktivitesine ters yönde olanı) olanında (3'¬¾ 5') sentezi kolayca ve kesintisiz olarak sürdürür. Çünkü, sentezlenecek olan yeni iplikçiğin yönü 5' ¾® 3' dür, yani enzimin aktivitesi yönündedir. Halbuki, açılan diğer parental iplikçiğin yönü 5' ¾® 3' polarite gösterir. Bunun karşısında sentezlenecek olan yeni iplikçiğin yönü ise, enzimin aktivitesine ve işleyişine ters bir durum gösterir (3' ¬¾ 5'). Bu iplikçikteki polimerizasyon kesintilidir, primerler ve okazaki segmentleri (1000-2000 bazlık DNA molekülü) yardımları ile gerçekleştirilir. Replikasyonun ileri aşamalarında RNA primerleri çıkartılarak bunların yerleri DNA ile doldurulur ve aralıkları DNA ligaz ile kapatılır, ve sentez her iki iplikçikte aynı anda tamamlanır. Çift iplikçikli DNA'nın replikasyonu, aynı bakterilerde olduğu gibi, semikonservatiftir.
Viral DNA'lar yapısal değişiklikler (tek iplikçik, çift iplikçik lineer, sirküler) gösterdiklerinden bunların replikasyonları arasında da bazı farklar bulunmaktadır.
Aşağıda bazı DNA virus familyalarında replikasyon mekanizmaları özetle verilmektedir.
Adenoviridae: Çift iplikçikli ve lineer bir genoma sahip olan adenoviruslarında, her iplikçiğin 5' terminusunda tersine tekrarlanan sekanslar (TIR, terminal inverted repeat) bulunur ve her uç kovalent olarak bir proteinle birleşmiştir. Bu proteinlerin prokürsörleri, Adeno viral DNA'nın sentezi için primer oluştururlar. Replikasyon, genomun iki ucundan başlar ancak asinkronize (asimetrik) bir tarzda 5' ¾® 3' yönünde devam eder. Reaksiyonu viral DNA polimeraz enzimi katalize eder. Sentez sırasında okazaki segmentleri meydana gelmez. Adenovirusları hücrelerin çekirdeklerinde replike olurlar. Tüm replikasyon için iki saat kadar bir süre geçer. Hücrelerin parçalanması ile viruslar dışarı çıkarlar.
Hepadnaviridae: Bu gruba ait virusların replikasyonları hücre çekirdeğinde gerçekleşir. Hepatitis B virusunun %70'i çift ve %30'u da tek iplikçik halindedir (ds/ssDNA). Lineer ve çift iplikçikli bir özelliğe sahip olan viral genom, viral DNA polimeraz enzimince, önce tam çift iplikçikli hale dönüştürülür ve sonra da sirküler forma çevrilir. Bu replikatif formun negatif polariteli olanı kalıp olarak kullanılarak sellüler RNA polimeraz II enzimi tarafından transkripte edilir ve tüm genom uzunluğunda "pregenom RNA" meydana getirilir. Böylece oluşturulan pozitif polariteli RNA molekülünden bu defa revers transkriptaz enziminin (RNA'ya bağımlı DNA polimerase) katalitik etkisi ile negatif sense DNA'lar sentezlenirler. Bunlar da çift iplikçikli DNA için kalıp ödevi görürler, Böylece, tek iplikçik bölgelere sahip çift iplikçikli (ds/ss DNA) infeksiyöz virus partikülleri oluşur.
Virionun tam serbest olmadığı durumlarda başlayan replikasyonlarda kısmi pozitif iplikçik DNA'lar sentezlenir.
Herpesviridae: Nukleusda replike olan ve çift iplikcikli lineer bir forma sahip olan herpesvirusları, diğer DNA viruslarından daha fazla enzime gereksinim duyarlar. Bunların bir bölümü hücre ve diğer bir kısmı da viral orijinlidir. Bu enzimler arasında, DNA polimeraz, helikaz, primaz, tek iplikçik DNA bağlayan proteinler (SSBP, destabilizan proteinler), replikasyon orijinini belirleyen ve tanıyan proteinler ve diğerleri bulunmaktadır.
Viral genom sitoplasmaya ulaştığında, çift iplikcikli sirküler forma dönüştürülür. Replikasyonun son aşamasında, rolling circle ve bu sirküler forma bağlı olarak gelişen lineer form (konkatamer formu) mekanizmalar etkinlik kazanır. Oluşan lineer form, enzimatik olarak belli yerlerinden (viral genom uzunluğunda) kesilerek projeni DNA molekülleri meydana gelir. Hücre içinde çok sayıda böyle formların oluşması, virus üretimini arttırır. Virusun transkripsiyon ve replikasyonu çekirdek içinde gerçekleşir.
Papovaviridae: Bu familyada bulunan DNA virusları çift iplikcikli sirküler bir özellik taşır ve hücrelerin nukleuslarında replike olurlar. Bu familya içinde iki cins (papillomavirus ve polyomavirus) bulunur. Polyomaviruslarından olan Simian virus 40 (SV40) üzerinde yapılan çalışmalar bu virusların ekspresyon ve replikasyon mekanizmaları üzerinde değerli bilgiler elde edilmiştir. SV40 virusunun replikasyonunda hücre orijinli DNA polimeraz alfa enziminin rolü önemlidir. Çift iplikcikli sirküler DNA'ya sahip olan bu viruslarda replikasyon bidireksiyonal olarak aynı anda başlar ve devam eder. Replikasyon çatalında kesintili ve kesintisiz sentez mekanizmaları meydana gelir ve kesintili olanında da okazaki segmentleri oluşur.
Parvoviridae: Tek iplikçik lineer bir genoma sahip olan parvovirusları hücre içine girdikten sonra, tek iplikçik ve lineer olan genomik DNA, çift iplikcikli sirküler replikatif forma dönüştürülür (çekirdek içinde). Burada transkripsiyon ve replikasyon gerçekleştirilir. Replikatif formlarda 5'-terminusunda meydana gelen kopmalar sonu tek iplikçik konkatamerler gelişir. Bunlar da enzimatik olarak kesilerek tek iplikçik lineer DNA molekülleri meydana gelir. Negatif sense tek iplikçik DNA'lar ayrı ayrı kapsidler içine paketlenirler.
Poxviridae: Çift iplikcikli lineer bir özellik gösteren poxvirusları DNA'larının bütün ekspresyon ve replikasyon aşamaları sitoplasma içinde cereyan eder. Virusun replikasyonunda hem hücre hem de virusa ait proteinlerden yararlanılır. Replikasyon virusun iki ucundan başlar devam ettirilir.
06.02. RNA Viruslarında Replikasyon
RNA viruslarının replikasyonlarını tam olarak tanımlamak oldukça güçtür. Viral genomun mRNA (pozitif polariteli RNA veya negatif polariteli RNA) olması, tek iplikcikli çift iplikcikli, segmentli-segmentsiz olmaları bunların replikasyonlarına etkilemekte ve değişik stratejiler kullanmalarına yol açmaktadır. RNA viruslarının replikasyonu, infekte ettiği hücrelerde bulunmayan veya sentezlenmeyen, bu nedenle de viral genom tarafından kodlanan RNA polimeraz enzimi (RNA'ya bağımlı RNA polimeraz, replikaz) tarafından katalize edilerek gerçekleştirilir. Enzim aynı zamanda, viral ekspresyonda da görev yapar (transkriptaz). RNA polimerazın bir özelliği de, primer olmaksızın sentezi başlatabilmesi ve devam ettirmesidir. Ancak, picornaviruslarında genomun 5' -terminal ucuna bağlanmış viral protein (Vgp) yeni iplikçik sentezinde primer oluşturur. RNA hücre içinde çok çabuk ayrıştırıldığı için, RNA polimeraz enzimi, virus zarflarından ayrılır ayrılmaz, hemen viral RNA'nın sentezine başlar. Bu enzim viral RNA'yı kalıp olarak kullanarak buna komplementer RNA sentezler ve bu da viral RNA'nın oluşturulması için kalıp fonksiyonu yapar.
Bazı RNA viruslarındaki replikasyon yandaki şekilde gösterilmektedir. | 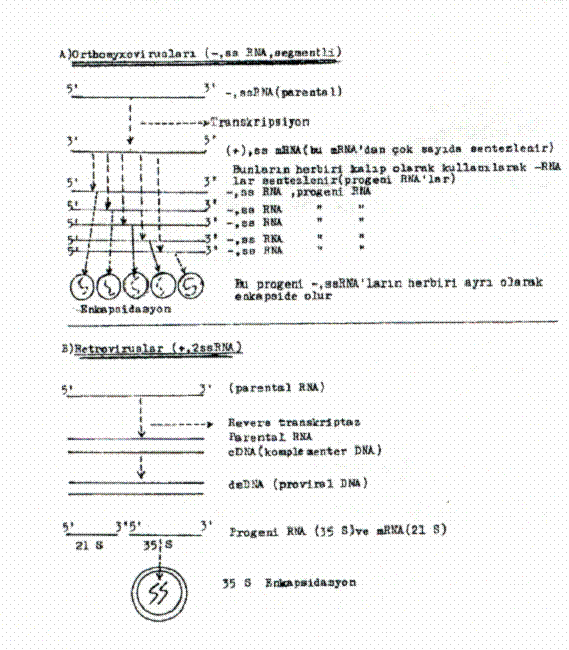 |
Viral genomların pozitif veya negatif polariteli, tek veya çift iplikcikli olduklarına göre replikasyonları arasında bazı farklar bulunmaktadır.
1) Negatif sens (polarite) tek iplikcikli RNA viruslarında (-,ss RNA): Böyle genoma sahip viruslarda (orthomyxovirus, paramyxovirus, rhabdovirus, filovirus, arenavirus ve bunyaviruslar) viral RNA'ya hücre içinde pozitif sens komplementer RNA sentezlenir. Bu + RNA, viral proteinlerin sentezi için m RNA aktivitesi gösterir ve aynı zamanda, negatif RNA'ların sentezi için de kalıp ödevi görür. Sentezlenen-RNA'lar projenileri oluşturur ve zarf içine paketlenir.
2) Pozitif, iki molekül tek iplikcikli RNA viruslarında (+ 2 ssRNA): Bu grupta bulunan Retroviruslarında, genomik RNA'nın taşıdığı revers transkriptaz enzimi (RNA'ya bağımlı DNA polimeraz) viral RNA'yı çift iplikcikli proviral DNA'ya (pro virus DNA) çevirir. Bu çift iplikçik ve sirküler olan proviral DNA hücre çekirdeğine girerek hücre kromozomuna integre olur. Burada hücre enzimlerince (RNA pol II) transkripte edilir ve oluşan tam uzunluktaki RNA'lar proses edilerek bunlardan gag, pol., ve env., RNA'lar oluşur. Bunlar sonradan birleşerek yeni virionu meydana getirirler. Ancak, proses edilen RNA'lar dan 35 S olanı pozitif projeni RNA'yı (genomu), diğeri ise (21 S) m RNA'yı teşkil eder.
3) Pozitif sens tek iplikcikli RNA viruslarında (+, ss RNA): Bu tarzda genoma sahip olan (picornaviruslar, caliciviruslar, togaviruslar, flaviviruslar ve coronaviruslar) viruslarda genom pozitif sens olduğu için (+ RNA), mesenger RNA (mRNA) aktivitesi gösterir. Direkt olarak ribosomlara bağlanarak translasyona tabi tutulur ve protein sentezi sağlanır. Pozitif RNA, kalıp olarak kullanılarak, RNA polimeraz enzimi tarafından negatif RNA'lar oluşturulur. Bu RNA'lar, replikatif intermediatları teşkil ederek bunlardan fazlaca projeni + RNA'lar meydana getirilir ve bunlar enkapside olurlar.
4) Çift iplikcikli segmentli RNA viruslarında (± ds RNA): Böyle genoma sahip viruslarda (reoviruslar), her segmentin negatif olanı kalıp olarak görev yapar ve bundan pozitif sens tek iplikçik RNA molekülleri sentezlenir. Bunlar hem mesenger aktivitesine sahiptirler ve hem de negatif polariteli projeni RNA'nın ikinci iplikçiğini oluşturmak için kalıp fonksiyonu yaparlar. Böylece çift iplikcikli ± tRNA projeniler meydana gelir ve bunlar enkapside olurlar.
Bazı RNA viruslarındaki replikasyon yandaki şekilde gösterilmektedir. | 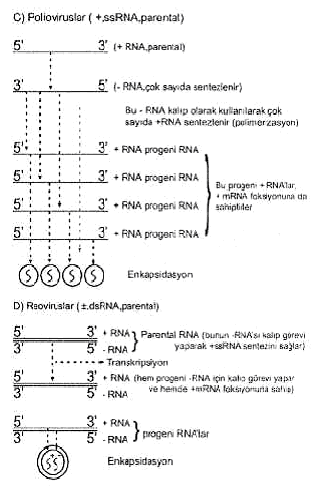 |
07. Viral Komponentlerin Sentezleri Ve Birleştirilmesi (Asamble)
Hücre içinde virus komponentlerin sentezinden sonra, bunların tam bir olgun veya infeksiyöz virusu oluşturacak tarzda, bir sıra ve düzen içinde bir araya getirilmesi kısa zamanda tamamlanır. Asamblede rol alan ve enerji sağlayan bazı spesifik proteinler bulunmaktadır.
Viral kapsidler boş olarak hücrenin çeşitli yerlerinde sentezlenirler ve bu aşamadan sonra viral genom kapsid içine paketlenirler.
Genetik materyallerin kapsid içine girmesinde özel proteinler fonksiyoneldir.
07.01. İkosahedral (kübik simetri) Viruslarda
Kübik simetrili viruslarda kapsidi oluşturan kapsomerler hücre içinde ayrı yerlerde hazırlandıktan sonra spontan olarak belli bir şekli oluşturmak üzere bir düzen ve sıra içinde yan yana gelir ve kovalent bağlarla birleşerek boş kapsidi (prokapsid) meydana getirirler. Hücrede, daha önce sentezlenen nukleik asitler de, paketleyici özel proteinler yardımı ile, boş kapsidlerin içine girerler (enkapsidasyon). Ancak, bazı kapsidler boş kalabildiği gibi, kapsid yapısında da defektler bulunabilmektedir.
İkosahedral viruslar DNA (herpes viruslar, adenoviruslar, papovaviruslar parvoviruslar) veya RNA (picornaviruslar, togaviruslar, flaviviruslar, calici viruslar, reoviruslar) karakterinde zarflı veya zarfsız olduklarına göre kapsomerlerin ve kapsidin sentez yerleri ve asamble bölgelerinde değişiklik olabilmektedir.
Adenoviruslarda, kapsomerler sitoplasmada sentezlenirler ve buradan nukleusa geçerek çekirdek içinde birleştirilerek kapsidi oluştururlar. Viral genom, henüz kapanmamış olan kapsidin içine paketlenir. Herpesviruslarında, nukleokapsid nukleus içinde asamble edilir ve nükleer membrandan tomurcuklanarak sitoplasmaya transfer edilir. Parvoviruslarda da kapsid formasyonu nukleus içinde gerçekleştirilir. Papovavirusları da, parvovirusları gibi genom kapsid içine nukleusda girer.
RNA viruslarından olan picornaviruslarında kapsid formasyonu sitoplasmada gerçekleştirilir ve viral genom burada kapsid içine paketlenir.
07.02. Helikal Simetrili Viruslarda
Zarflı helikal simetriye sahip olan viruslarda (coronaviruslar, paramyxoviruslar, rhabdoviruslar, bunyaviruslar, arenaviruslar) sitoplasmada sentezlenen kapsomerler RNA üzerinde yan yana gelerek helikal simetri oluştururlar. Bütün viral komponentler, sentezi ve asamble işlemleri sitoplasmada gerçekleşir. Zarf, hücre membranlarından çıkarlarken viriona katılır.
07.03. Kompleks Yapılı Viruslarda
Poxviruslarında ekspresyon, replikasyon ve viral komponentlerin asamblesi sitoplasmada gerçekleştirilir.
08. Virusların Olgunlaşması (Maturasyon)
İkosahedral viruslarda, viral genomun önceden hazırlanmış olan boş kapsidin içine girmesi ile olgunlaşma tamamlanmasına karşın, zarflı viruslarda olgunlaşma daha değişik bir tarzda gerçekleştirilir. Özellikle, helikal simetriye sahip olan zarflı viruslar hücre membranlarından çıkarken tomurcuklanma sırasında membranlardan aldıkları lipid katmandan oluşan bir zarfla kaplanarak olgunlaşırlar.
Herpes virusları hücre çekirdeğinde enkapside olduktan sonra, çekirdekten tomurcuklanma ile çıkarlarken nükleer membrandan da bir kısım alarak sitoplasmaya transfer olur. Virus partikülleri hemen Golgi aparatına gelir. Burada glikoproteinler proses edildikten sonra ekzositozis ile veya hücrelerin lize olması ile de dışarı çıkabilirler.
Matriks proteinine sahip olmayan bazı viruslar (flaviviruslar, coronaviruslar, bunyaviruslar) granüler endoplasmik retikulum (GER) veya Golgi aparatından tomurcuklanma ile olgunlaşarak sitoplasmaya ulaşır ve burada özel vesiküllere bağlanarak plasma membranına gelirler ve ekzositozisle dışarı çıkarlar.
Çiçek virusları etrafındaki katmanlarının sentezi viral genom tarafından kodlanır, hücreye ait bir materyal taşımaz. Poxvirusları sitoplasmada replike olur ve olgunlaşır.
Birçok zarflı virus türleri hücre membranlarından ve bazıları da internal membranlardan (nükleer membran, Golgi aparatı, endoplasmik retikulum) tomurcuklanarak olgunlaşırlar. Şöyle ki, tomurcuklanmanın meydana geleceği yerde plasma membranında peplomerler (dışta) ve iç kısmında da matriks proteinleri birikmeye başlar: Bu aşamadan sonra da nukleokapsid gelerek, sitoplasmik membranın alt kısmına yerleşir. Hücre membranında oluşan dışarı doğru kabarma giderek artar, bir tomurcuk gelişir ve bu tomurcuk (olgunlaşmış virus) etrafına hücre membranından bir zarf oluşur. Böylece olgunlaşan virus hücre membranından ayrılır ve serbest kalır.
Tomurcuklanma ile olgunlaşmada ve çıkışta, hücrelerde bir zarar oluşmamaktadır. Çünkü, hücre membranı hemen tamir edilmekte, hücreler normal yaşamlarına ve çoğalmalarına devam etmektedirler. Böyle karaktere sahip viruslar, genellikle, non sitopatiktirler ve persistent infeksiyonlara yol açarlar.
Zarflı viruslarda, zarfın yüzeyinde lokalize olan peplomerler (spike) virus tarafından kodlanırlar. Yapıları protein, glikoprotein olmaları nedeniyle de antijeniktirler (hemaglutinin, neuraminidase, F-proteini) ve vücutta antikor sentezini uyarırlar.
09. Virusların Hücrelerden Çıkışları (Serbest Kalma)
Hücrede çeşitli tarzlarda olgunlaşan ve infeksiyöz bir karakter taşıyan zarfsız veya zarflı viruslar (virion) başlıca 3 mekanizma ile dışarı çıkmaktadırlar.
Virusların hücreden çıkışları yandaki şekilde gösterilmektedir. | 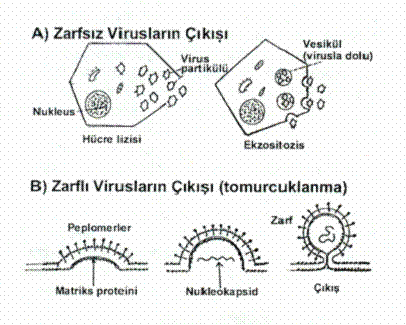 |
09.01. Hücrelerin Ölmesi (Sitolizis)
İkosahedral simetriye sahip bazı viruslar da üreme hem çabuktur ve hem de hücrelerde ölümler meydana gelir (litik etki, sitolitik etki). Hücrelerin parçalanması ile serbest kalan viruslar hücrelerden dışarı çıkarak başka sağlam hücreleri infekte ederler. Picornaviruslarında, virionun oluşumundan hemen sonra hücrelerde parçalanma meydana gelir. Nukleusda olgunlaşan bazı viruslarda, bir süre çekirdek içinde kalabilir ve çekirdek parçalanınca ekstrasellüler ortama çıkarlar. Herpesvirusları ise hem hücrelerin parçalanması ve/veya ekzositozisle dışarı salınabilirler.
09.02. Tomurcuklanma
Bazı helikal simetrili viruslarda (paramyxoviruslar orthomyxoviruslar, rhabdoviruslar, arenaviruslar,) hücrelerden tomurcuklanma ile dışarı çıkarlar. Böyle hücreler, genellikle, hücrelerde parçalanma (CPE) oluşturmazlar, hücreler normal yaşamlarına devam ederler ve persistent infeksiyonlara da yol açabilirler.
09.03. Ekzositozis
Bazı zarflı viruslar (coronavirusları, bunyaviruslar, flaviviruslar) ile herpes viruslarında sitoplasmadan çıkış ekzositozis ile olmaktadır. Sitoplasmada serbest halde bulunan viruslar, bazı özel vesiküllere bağlanarak hücre membranına ulaşırlar ve membrandan dışarı ekzositozis ile çıkarlar.
Aşağıdaki tabloda bazı virus familyalarında replikasyon yerleri, eklips periodu ve çıkış tarzları (membranlar) gösterilmektedir.
Virus | Replikasyon | Eklips | Çıkış tarzları |
familyası | yeri | periodu | (membran) |
| | (saat) | |
Parvoviridae | Nukleus | 6 | - |
Papovaviridae | Nukleus | 13 | - |
Adenoviridae | Nukleus | 10 | - |
Herpesviridae | Nukleus | 4 | Nukleer membran |
Poxviridae | Sitoplasma | 4 | Golgi aparatı |
Picornaviridae | Sitoplasma | 2 | - |
Caliciviridae | Sitoplasma | 3 | - |
Togaviridae | Sitoplasma | 2 | Plasma membranı |
Flaviviridae | Sitoplasma | 3 | Endoplasmik |
| | | retikulum |
Coronaviridae | Sitoplasma | 5 | Golgi |
Paramyxoviridae | Sitoplasma | 4 | Plasma membranı |
Rhabdoviridae | Sitoplasma | 3 | Plasma membranı |
Arenaviridae | Sitoplasma | 5 | Plasma membranı |
Bunyaviridae | Sitoplasma | 4 | Golgi |
Orthmyxoviridae | Nukleus | 4 | Plasma membranı |
Reoviridae | Sitoplasma | 5 | |
Birnaviridae | Sitoplasma | 4 | |
Retroviridae | Nukleus | 10 | Plasma membranı |
| | | |
| | | Fenner, 1993 |
Virus | Viral | Genom | Nukleo- | Virion | Multip- |
familyası | protein | replikas- | kapsid | olgunlaşma | likasyon |
| sentez | yon yeri | formasyon | yeri | süresi |
| yeri | | yeri | | (saat) |
Parvoviridae | S | N | N | N | |
Papovaviridae | S | N | N | N | 48 |
Adenoviridae | S | N | N | N | 25 |
Hepadnaviridae | S | N | S | M-E | |
Herpesviridae | S | N | N | M | 15-72 |
Poxviridae | S | S | S | S | 20 |
Picornaviridae | S | S | S | S | 6-8 |
Reoviridae | S | S | S | S | 15 |
Togaviridae | S | S | S | M-P | 10-24 |
Flaviviridae | S | S | S | M-E | |
Retroviridae | S | N | S | M-P | |
Bunyaviridae | S | S | S | M-G | 24 |
Orthomyoxoviridae | S | N | N | M-P | 15-30 |
Paramyxoviridae | S | S | S | M-P | 10-48 |
Rhabdoviridae | S | S | S | M-P | 6-10 |
Jawetz, 1998 |
S: Sitoplasma, N: Nukleus, M: Membran |
M-E: Membran, endoplasmik retikulum |
M-G: Membran-golgi, M-P: Membran-plasma membranı |
[1] Kaynak : Temel Mikrobiyoloji